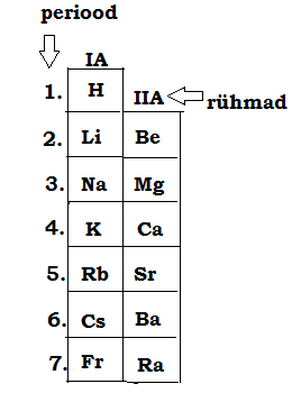
Perioodis vasakult paremale jääb elektronkihtide arv samaks, kuid iga järgmise elemendi tuumalaeng ja väliskihi elektronide arv aatomis on ühe võrra suurem.
Rühmas ülevalt alla jääb väliskihi elektronide arv samaks, kuid iga järgmise elemendi elektronkihtide arv aatomis on ühe võrra suurem- seetõttu kasvavad rühmas ülevalt alla aatomite mõõtmed.
Elektronskeemi koostamine:
- 1. elektronkiht - kuni 2 elektroni
- 2. elektronkiht – kuni 8 elektroni
- 3. elektronkiht – kuni 18 elektroni
- 4. elektronkiht – kuni 32 elektroni
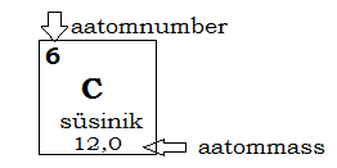
Nt: Mg- magneesium
Magneesiumi aatomnumber/ järjekorra number on 12- tal on kokku 12 elektroni.
Magneesium asub kolmandas perioodis, seega on tal kokku kolm elektronkihti, ja IIA rühmas, seega on tema väliskihil 2 elektroni. Kuna esimeses elektronkihis saab olla maksimaalselt 2 elektroni, siis saame välja arvutada ka teise elektronkihi elektronide arvu 12-2-2=8
Seega Mg +12丨2) 8) 2)
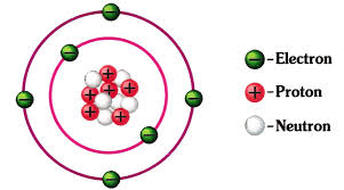
Arvutame ka magneesiumi prootonite, elektronide ja neutronite arvu.
prootonite arv 12 ( järjekorra number)
elektronide arv 12 ( järjekorra number)
neutronite arv 24,31- 12= 12,31 ~ 12 ( aatommass- prootonite arv)
Harjuta ka siin :
http://www.hot.ee/vanavares/elektronskeem/elektronkihid2.htm